实验室环境设施要求:
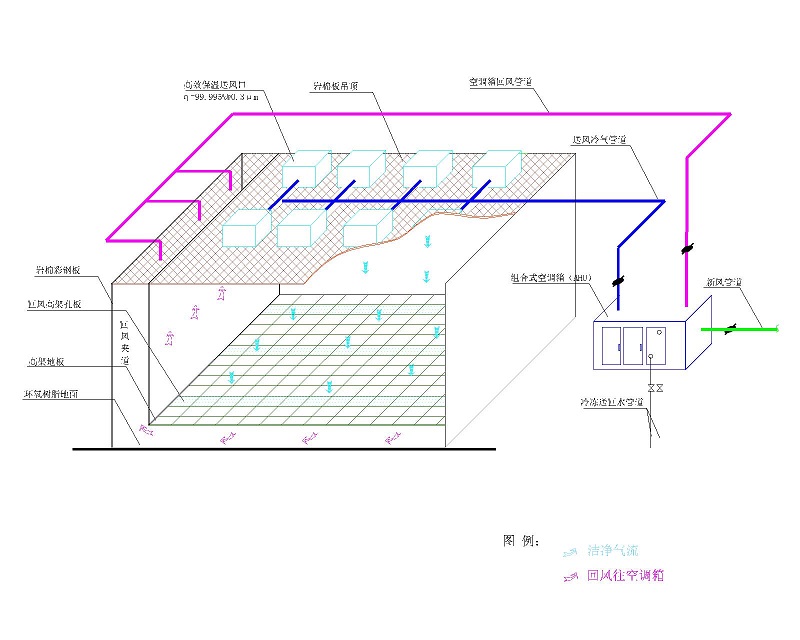
无菌操作室的环境洁净度条件不应低于无菌生产操作区,以降低无菌检查出现假阳性的风险。无菌检查应在环境洁净度10000级下的局部洁净度100级的单向流空气区域内或隔离系统中进行。
无菌室分无菌操作室和缓冲间。无菌操作室应具有空气除菌过滤的单向流空气装置。操作室或工作台应保持正压。应在压差十分重要的相邻级别区之间安装压差表。
微生物限度检查宜在环境洁净度10000级下的局部洁净度100级的单向流空气区域内进行;
系统设计考虑因素
检验、中药标本、留样观察以及其他各类实验室应与药品生产区分开。
抗生素微生物检定实验室、放射性同位素检定室的空气洁净度等级不宜低于C级。
实验室净化空调系统应与药品生产区严格分开。
阳性对照室和放射性同位素检定室等实验室不应利用回风,室内空气经过滤后直接排至室外。
有活性和放射性物质的实验室的空气要直排,并经高效过滤器;而且要有正压气锁等防止室内空气外逸等措施。
无菌检查室、微生物限度检查实验室、抗生素微生物检定实验室当各自单独设置空调系统时均可以各自单独回风,但若集中合并为一个空调系统时,抗生素微生物检定实验室的空气需直排,不能利用回风(抗生素的微生物会影响无菌检查室、微生物限度检查实验室菌种的培养)
检验、留样观察以及其他各类实验室应与药品生产区分开设置。
阳性对照、无菌检查、微生物限度检查和抗生素微生物检定等实验室,以及放射性同位素检定室等应分开设置。
无菌检查室、微生物限度检查实验室应为无菌洁净室,其空气洁净度等级不应低于B级,并应设置响应的人员净化和物料净化设施
微生物实验室一般由准备间、操作间、灭活间、无菌操作间和设备间等构成。
操作间一般应包括无菌检查室、微生物限度检查室和阳性对照室、生物检定室、细菌内毒素检查室(不需要无菌操作条件)、不溶性微粒检查室(*容易忽视的无菌室)。对要求无菌的,如注射剂、眼用制剂等需要在无菌室中进行检测,可采用万级洁净环境下设置超净工作台来实现;对不要求完全无菌的一般制剂,又不允许某些菌的存在,并且对于允许存在的菌落数又加以限制,如:内服固体制剂、内服液体制剂、外用制剂等,在无菌室中进行检测,可采用在十万级洁净环境下设置超净工作台来实现。微生物实验室同时还应设置配套的培养间、准备间、清洗间、灭菌间等。












